CPhIセミナーレポート:医薬品(原薬)中の変異原性不純物 ~試験法開発及び分析例~
2022.06.02
CPhI Japan2022において、開発分析研究本部 井上裕太より、ICH M7対応について、ブース内プレゼンテーションを致しました。当日の内容について、ご紹介します。
ICH M7について
ICH M7は、潜在的発がんリスクを低減するための医薬品中DNA反応性(変異原性)不純物の評価及び管理について示されたガイドラインである。
ICH M7において、不純物の評価は2段階の過程で行われる。
第1段階:構造が決定されている実際の不純物についての変異原性を評価
第2段階:潜在的な不純物が最終原薬中に存在する可能性を評価し、変異原性についての更なる評価の必要性を判断
原薬および製剤中の不純物は以下の5つのClassに分類され、それぞれ管理対応基準が定められている。
Class2とClass3の不純物は、投与期間に応じて許容1日総摂取量として許容限度値(TTC*)が設定されている。
Class2またはClass3の不純物が3つ以上存在する場合は、両方の基準を満たす必要がある。
*TTC=Thresholds of Toxicological Concern
なお、TTCを下回る摂取量であっても、理論的に著しい発がんリスクの可能性を伴うと考えられる化合物(これらを「Cohort of Concern」と呼ぶ)として以下の3グループの化合物群があり、これらは特に管理が必要である。
-アフラトキシン様化合物
-N-ニトロソ化合物
-アルキルアゾキシ化合物
不純物の管理方法の決定は、1. 不純物の洗い出し、2. 不純物の分類、3. 不純物の管理方法の決定、のプロセスで進めるが、これを効率的に実施するためには分析化学者とプロセス化学者の協働で行う必要がある。
ICH M7では不純物の管理戦略として4つのオプションが示されている。特にoption 1,2が選択されるものについては、高感度分析法の設定が必須となる。
なお、不純物の管理を最小限かつリスクを低減するために、まず原薬への混入リスクを避ける(原料・中間体で規格化する)ことが必要である。
また、どの工程で管理するかは、対象化合物の物性に加えて、合成プロセスの管理戦略に依存するプロセス化学者との協働で丁寧に行う必要がある。
微量分析法開発のために
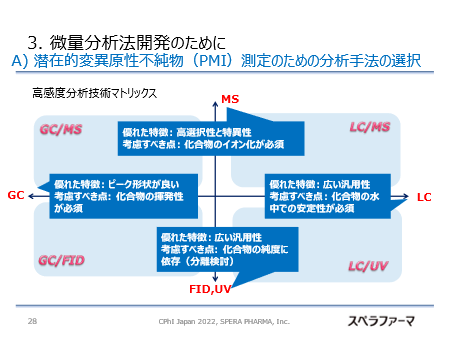
スペラファーマは、潜在的変異原性不純物(以下、PMI)の高感度分析として、以下のような分析手法のマトリックスを用いて、化合物の特性(イオン化するかどうか、分離検討が必要か、揮発性があるかどうか、溶液中での安定性など)に適した分析手法を効率的に選択している。
スペラファーマにおける分析法設定事例
LC/UV
– アルキルスルホネート Threshold 2 ppmでの測定可能な分析手法を開発
LC-MS
– ブロモ酢酸 Threshold 10 ppmでの測定可能な分析手法を開発
– 類縁物質 Threshold 10 ppmの4つの類縁物質を同時に測定
– 類縁物質 Threshold 0.9 ppmという高感度の分析手法を開発
GC-MS
– アルキルトシレート Threshold 3 ppmでの測定可能な分析手法を開発
– メタンスルフォニルクロライド Threshold 10 ppmでの測定可能な分析手法を開発
– エタンスルフォニルクロライド Threshold 3 ppmでの測定可能な分析手法を開発
– ベンザルクロライド Threshold 0.75 ppmでの高感度な分析手法を開発
ヘッドスペースGC-MS
– ベンゼン Threshold 0.6ppmでの測定可能な分析手法を開発
– N-ニトロソジメチルアミン Threshold 40 ppbでの超高感度の分析手法を開発
– N-ニトロソジエチルアミン Threshold 0.4 ppmでの測定可能な分析手法を開発
ICP-AES、ICP-MS
– ホウ素化合物 LC/UVで検出が困難であったPEBの測定法を開発(Threshold 10 ppm)
おわりに
原薬・製剤の不純物管理での薬事規制当局対応には、高感度分析法は不可欠である。
スペラファーマは、原薬の品質を保証するためには、どの工程でPMIsを管理するのが効果的であるかを、原薬プロセス化学者と分析化学者が協力して不純物の管理戦略を立案し、PMIsの特性に応じた高感度分析技術を提供することが可能である。
スペラファーマでは、これまでPMIsの残存を10 ppm以下で保証できる300種以上の分析法を確立してきた。今後、ますます厳しくなっていくと見込まれる薬事規制当局の要求事項に対しても、適切に対応していくことが可能である。
―――――――――――
ご質問などございましたら、問い合わせフォーム(https://www.spera-pharma.co.jp/inquiry/)よりご連絡をお願い致します。
page top